Apa materi kimia yang Anda sukai? Ingatkah Anda pada materi sel elektrolisis? Ya, elektrolisis adalah materi yang banyak disukai siswa karena sangat dekat dengan keseharian dan siswa dapat melakukan banyak percobaan.
Salah satu contoh sederhana dari penerapan prinsip kerja elektrosis adalah aki kendaraan bermotor. Aku merupakan komponen penting pada motor maupun mobil, karena keduanya membutuhkan aki agar mesin menyala. Tapi tahukah Anda bagaimana proses pengisian ulang energi kimia pada aki? Jadi, proses pengisian ulang tersebut menggunakan prinsip kerja yang disebut dengan sel elektrolisis. Teruslah membaca untuk mengetahui lebih banyak!
Apa itu sel elektrokimia? Pengertian sel elektrokimia sendiri adalah sebuah alat yang dapat menghasilkan energi listrik dari reaksi kimia atau sebaliknya.
Artikel ini sedikit banyak akan membahas pengertian dari sel elektrolisis, komponen-komponen pada sel elektrolisis tersebut (katoda dan anoda), prinsip kerja, serta soal eletrolisis yang dapat membantu Anda belajar kimia lebih mudah dan menyenangkan.
Jika Anda merasa kesulitan dalam mempelajari kimia, ini saat yang tepat untuk Anda bergabung dalam kursus privat Superprof
Cek di sini untuk mempelajari titik didih

Pengertian Sel Elektrolisis
Sel elektrolisis adalah reaksi yang mengubah energi listrik menjadi energi kimia. Sel ini merupakan sel elektrokimia yang digunakan untuk mendorong reaksi redoks non-spontan lewat penerapan energi listrik. Proses elektrosis adalah 'untuk memutuskan' dalam bahasa Yunani, yang artinya dalam hal ini elektrolisis digunakan untuk mengurai zat atau senyawa kimia dengan memanfaatkan arus listrik. Sederhananya, sel elektrolisis merupakan bagian dari sel elektrokimia, yang menggunakan energi listrik untuk menjalankan reaksi redoks tidak spontan.
Perbedaan Sel Elektolisis dan Sel Volta
Sel elektrolisis dan sel volta memiliki perbedaan yang cukup terlihat jelas. Seperti dilansir laman Chemistry LibreTexts, perbedaan utama sel volta dan sel elektrolisis yaitu:
1. Definisi sel volta adalah sel elektrokimia yang mengubah reaksi kimia menjadi listrik, mengandung anoda negatif dan katoda positif, pada reaksi redoks sel volta menampilkan reaksi spontan. Fungsi sel volta sendiri yaitu mengubah energi kimia jadi energi listrik melalui suatu reaksi elektrokimia redoks spontan. Fungsi tersebut telah banyak dimanfaatkan dalam kehidupan sehari-hari, terutama dalam pembuatan jenis baterai, seperti sel kering, baterai alkali, sel aki, dan baterai litium.
2. Sedangkan sel elektrolisis adalah sel elektrokimia yang mengubah arus listrik jadi energi kimia, reaksi redoks nya non-spontan, dan mengandung anoda positif dan katoda negatif.
Komponen-komponen sel elektrolisis
Komponen yang ada dalam sel elektrolisis adalah elektroda (anoda dan katoda), elektrolit dan juga sumber listrik.
Elektroda
Komponen sel elektrolisis yang pertama adalah elektroda. Elektroda merupakan konduktor listrik berupa logam yang terdiri dari dua bagian, yaitu elektroda positif dan negatif. Elektroda positif disebut dengan anoda, sedangkan elektroda negatif disebut dengan katoda. Pada penjelasan selanjutnya, Anda akan menemukan definisi lebih lengkap tentang katoda dan anoda pada elektrolisis.
Katoda
Katoda adalah elektroda bermuatan listrik negatif yang berfungsi sebagai tempat terjadinya reaksi reduksi pada sel elektrolisis. Elektron dari sumber listrik akan memasuki katoda dan mereduksi ion di dalamnya. Ion yang direduksi kemudian akan menghasilkan endapan logam pada katoda. Makin besar muatan listriknya, maka makin banyak juga endapan logam yang terbentuk.
Pada sel elektrolisis terdapat 2 elektroda yang dihubungkan pada sumber listrik yaitu anoda di kutub positif dan katoda di kutub negatif. Anoda pada sel elektrolisis merupakan tempat terjadinya reaksi oksidasi, sedangkan katoda merupakan tempat terjadinya reaksi reduksi. Katoda sendiri terdiri dari katoda positif atau negatif. Adapun, contoh katoda yang kerap digunakan dalam sel elektrolisis adalah natrium.
Anoda
Anoda adalah elektroda bermuatan listrik positif yang berfungsi sebagai tempat terjadinya reaksi oksidasi pada sel elektrolisis. Pada anoda, reaksi oskidasi menyebabkan ion melepaskan elektron dan menghasilkan gas yang terlihat seperti gelembung pada anoda. Adapun, contoh anoda yang kerap digunakan dalam sel elektrolisis adalah klor dan seng.
Elektrolit
Elektrolit merupakan salah satu komponen utama sel elektrolisis. Dilansir dari Encyclopedia Britannica, elektrolit berfungsi mengangkut muatan listrik melalui migrasi ion. Penggunaan elektrolit dalam sel elektrolisis sangat penting, terutama saat elektroda inert yang digunakan.
Periksa di sini untuk mempelajari tentang termokimia
Reaksi Katoda dan Anoda
Pada sel elektrolisis, reaksi katoda dan anoda merupakan bagian penting dalam memahami proses ini.
- Reaksi yang terjadi di katoda adalah reaksi reduksi yang terjadi pada elektroda negatif (katoda). Elektron yang masuk ke katoda akan mereduksi ion-ion positif yang ada di sekitar katoda, yang akhirnya membentuk endapan logam atau gas tertentu. Sebagai contoh, pada elektrolisis lelehan NaCl, ion Na+ akan tereduksi di katoda membentuk logam Na.
- Reaksi yang terjadi di anoda adalah reaksi oksidasi yang terjadi pada elektroda positif (anoda). Ion-ion negatif yang mendekati anoda akan kehilangan elektron dan menghasilkan gas atau senyawa lain. Sebagai contoh, pada elektrolisis NaCl, ion Cl− akan teroksidasi di anoda membentuk gas Cl2.
Cara Menentukan katoda dan Anoda pada Sel Elektrolisis
Dalam proses elektrolisis, sangat penting untuk mengetahui cara menentukan katoda dan anoda agar reaksi elektrokimia dapat berlangsung dengan benar. Katoda dan anoda adalah dua elektroda utama dalam sel elektrolisis yang berfungsi untuk melakukan reaksi redoks. Untuk menentukan katoda dan anoda, langkah pertama yang perlu dilakukan adalah memahami sifat-sifat elektroda tersebut. Katoda adalah elektroda yang bermuatan negatif dan merupakan tempat terjadinya reaksi reduksi, di mana ion positif dari larutan akan menerima elektron dan tereduksi menjadi unsur atau senyawa yang lebih sederhana. Sebaliknya, anoda adalah elektroda yang bermuatan positif dan merupakan tempat terjadinya reaksi oksidasi, di mana ion negatif akan melepaskan elektron dan teroksidasi menjadi gas atau senyawa lainnya. Proses cara menentukan katoda dan anoda dapat ditentukan dengan melihat arah aliran arus listrik.
- Arus listrik selalu mengalir dari kutub positif ke kutub negatif, sehingga pada sumber listrik, kutub positif akan terhubung dengan anoda, dan kutub negatif akan terhubung dengan katoda.
- Pada elektrolisis, ion-ion dari larutan akan bergerak menuju elektroda yang sesuai dengan muatan lawannya. Sebagai contoh, pada elektrolisis air, ion H+ akan tereduksi di katoda membentuk gas hidrogen, sedangkan ion OH− akan teroksidasi di anoda membentuk gas oksigen. Oleh karena itu, untuk mempermudah pemahaman, dapat disimpulkan bahwa cara menentukan katoda dan anoda berkaitan erat dengan sifat muatan elektroda dan jenis reaksi yang terjadi di masing-masing elektroda.

Prinsip Kerja dan Penerapannya

Sel elektrolisis mempunyai dua elektroda bersifat negatif dan positif. Cara kerja sel elektrolisis yaitu dengan menghubungkan sumber arah dari kutub negatif ke katoda dan kutub positif ke anoda.
Kemudian terjadi over potential yang mendorong reaksi reduksi dan oksidasi non-spontan dapat berjalan. Sehingga elektron dapat mengalir dari katoda ke anoda dan ion-ion positif cenderung ke katoda lalu tereduksi. Sementara ion-ion negatif tertarik ke anoda dan teroksidasi.
Secara umum, elektrolisis lelehan senyawa ionik melibatkan reaksi redoks yang lebih sederhana. Hal ini dikarenakan tanpa adanya air, kation akan direduksi di katoda dan anion akan dioksidasi di anoda. Sebagai contoh, pada elektrolisis lelehan NaCl, ion Na+ akan tereduksi di katoda membentuk logam Na dan ion Cl− akan teroksidasi di anoda membentuk gas Cl2.
Namun, jika reaksi elektrolisis berlangsung dalam sistem larutan, ada beberapa reaksi redoks yang bersaing sehingga reaksi cenderung kompleks.
Cek di sini jika sedang ingin mempelajari struktur atom
Skema Eletrolisis
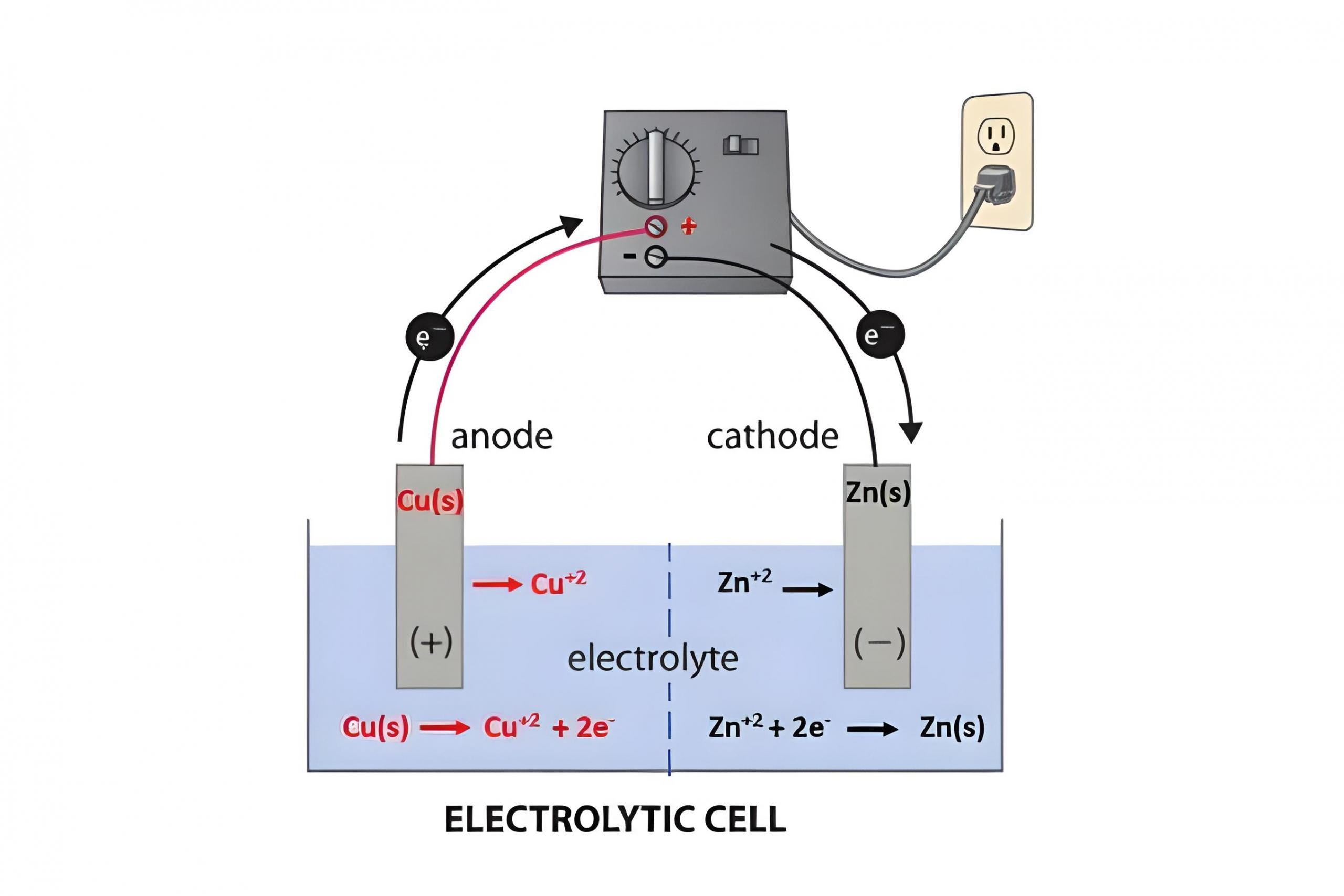
Untuk lebih memahami proses elektrolisis, berikut ini adalah skema eletrolisis yang menggambarkan aliran arus listrik melalui elektrolit, serta posisi anoda dan katoda:
- Anoda : Tempat terjadinya oksidasi, ion-ion di sini melepaskan elektron.
- Katoda : Tempat terjadinya reduksi, ion-ion di sini menerima elektron.
Skema elektrolisis ini menggambarkan proses pemisahan senyawa melalui arus listrik dengan peran masing-masing elektroda yang mempengaruhi hasil reaksi.
Fungsi Sel Elektrolisis Dalam Kehidupan
Apa fungsi atau kegunaan sel elektrolisis dalam kehidupan manusia? Berikut penjelasan dari kegunaan sel elektrolisis dalam kehidupan sehari-hari :
Proses sel elektrolisis biasa digunakan pada metode pembuatan gas oksigen, hidrogen, dan gas klorin di laboratorium.
2. Bermanfaat untuk proses dalam memurnikan logam yang kotor. Caranya adalah logam kotor ditempatkan pada anoda sementara logam murni pada katoda.
3. Sel elektrolis berguna dalam proses penyepuhan logam menggunakan logam mulia, misalnya perak, emas, dan nikel.
4. Membantu dalam proses produksi aluminium dan natrium.
Jadi, sel elektrolisis merupakan salah satu reaksi kimia yang penting dalam kehidupan sehari-hari. Hal ini menunjukkan bahwa setiap sel elektrokimia termasuk sel volta memiliki kegunaan dan perannya masing-masing.
Contoh Reaksi Elektrolisis
Elektrolisis larutan KI dengan elektrode grafit
KI(aq) → K+(aq) + I−(aq)
K termasuk logam golongan IA, sehingga air akan tereduksi di katode. Oleh karena elektrode grafit termasuk elektrode inert dan anion I− tidak termasuk sisa asam oksi, maka anion I− akan teroksidasi di anode.
Katode : 2H2O(l) + 2e− → H2(g) + 2OH−(aq)
Anode : 2I−(aq) → I2(g) + 2e−
Reaksi sel : 2H2O(l) + 2I−(aq) → H2(g) + 2OH−(aq) + I2(g)
Sel elektrolisis dapat diterapkan dalam kehidupan, berikut contoh penerapan reaksi sel elekrolisis yang menarik untuk diketahui adalah pelepuhan logam. Tentu saja ini menjadi penerapan yang sangat bermanfaat mengingat besi yang mudah berkarat sehingga penyepuhan logam menjaga besi agar tidak berkarat. Contohnya mata pisau yang dilapisi oleh perak. Berikut reaksi kimia untuk penyepuhan logam.
Penyepuhan Logam
Penyepuhan logam seperti pada sendok dan cincin perak dengan tujuan melapisi logam tersebut agar tidak berkarat. Ketika arus listrik dialirkan, maka akan terjadi reaksi, yaitu
Anoda : Ag Ag+ + e
Katoda : Ag+ + e Ag
Pada katoda akan menghasilkan Ag yang melapisi elektroda.
Cek di sini untuk mempelajari tentang pengenceran larutan
Contoh Soal Elektrokimia

Berikut adalah contoh soal elektrokimia yang dapat membantu Anda lebih memahami konsepnya:
- Sel Volta pada Reaksi Zn dan Cu
Soal: Sebuah sel volta terdiri dari dua elektroda: Zn dan Cu yang terendam dalam larutan ZnSO₄ dan CuSO₄. Tentukan arah aliran elektron dan reaksi yang terjadi pada masing-masing elektroda!
Jawaban:- Arah aliran elektron: Dari Zn ke Cu (melalui kawat luar)
- Reaksi pada katoda (Cu): Cu²⁺ (aq) + 2e⁻ → Cu (s)
- Reaksi pada anoda (Zn): Zn (s) → Zn²⁺ (aq) + 2e⁻
- Pengaruh Potensial Elektrode pada Sel Elektrokimia
Soal: Diketahui potensial standar elektroda untuk Cu²⁺/Cu adalah +0,34 V dan untuk Zn²⁺/Zn adalah -0,76 V. Tentukan EMF sel dari sel elektrokimia yang menggabungkan elektroda Cu dan Zn!
Jawaban:
EMF sel = E°(katoda) - E°(anoda)
EMF sel = 0,34 V - (-0,76 V) = 1,10 V - Sel Elektrokimia pada Reaksi Fe dan Ni
Soal: Pada sel elektrokimia yang terdiri dari elektroda Fe dan Ni yang terendam dalam larutan Fe²⁺ dan Ni²⁺, tentukan reaksi yang terjadi pada masing-masing elektroda!
Jawaban:- Arah aliran elektron: Dari Fe ke Ni (melalui kawat luar)
- Reaksi pada katoda (Ni): Ni²⁺ (aq) + 2e⁻ → Ni (s)
- Reaksi pada anoda (Fe): Fe (s) → Fe²⁺ (aq) + 2e⁻
Contoh Soal Reaksi Elektrolisis dan Soal Sel Elektrolisis
Tulislah reaksi elektrolisis berikut.
a. elektrolisis larutan CuSO4 dengan elektrode tembaga
b. elektrolisis larutan KI dengan elektrode grafit
c. elektrolisis lelehan CaCl2 dengan elektrode platina
Jawab:
a. CuSO4(aq) → Cu2+(aq) + SO42−(aq)
Cu tidak termasuk logam aktif, sehingga kation Cu2+ akan tereduksi di katode. Oleh karena elektrode tembaga (Cu) tidak termasuk elektrode inert, maka anode Cu akan teroksidasi.
Katode : Cu2+(aq) + 2e− → Cu(s)
Anode : Cu(s) → Cu2+(aq) + 2e−
Reaksi sel : Cu(s)anode → Cu(s)katode
b. KI(aq) → K+(aq) + I−(aq)
K termasuk logam aktif, sehingga air akan tereduksi di katode. Oleh karena elektrode grafit termasuk elektrode inert dan anion I−tidak termasuk sisa asam oksi, maka anion I−akan teroksidasi di anode.
Katode : 2H2O(l) + 2e− → H2(g) + 2OH−(aq)
Anode : 2I−(aq) → I2(g) + 2e−
Reaksi sel : 2H2O(l) + 2I−(aq) → H2(g) + 2OH−(aq) + I2(g)
Sebagai referensi, Anda bisa melihat tabel elektrolisis untuk memahami reaksi reduksi dan oksidasi yang terjadi pada katoda dan anoda
Setelah memahami pembahasan untuk poin (a) dan (b), sekarang cobalah untuk mengerjakan poin (c) dan diskusikan jawaban Anda pada kolom komentar!
Belajar kimia tentu akan lebih mudah dengan memahami konsep dan mencoba beberapa latihan soal. Anda juga dapat belajar bersama guru privat kimia untuk membangun suasana belajar yang lebih mudah dan menyenangkan. Temukan guru yang tepat di sekitar Anda hanya pada situs web online Superprof.
Ringkaskan dengan AI