Dalam pembahasan reaksi redoks, ada empat hal utama yang selalu terlibat: oksigen, hidrogen, elektron, dan perubahan nilai bilangan redoks. Kalau sudah masuk ke bagian bilangan oksidasi, sangat penting untuk memahami lebih dulu konsep dasarna. Dimulai dari apa itu biloks sampai aturan-aturan yang berlaku.
Di artikel ini, kita akan mengupas tuntas tentang bilangan oksidasi. Mulai dari definisi, cara menentukan bilangan oksidasi, hingga contoh soal biloks agar kamu semakin paham. Yuk, langsung kita bahas!

Pengertian Bilangan Oksidasi (Biloks)

Oksidasi adalah proses kimia di mana suatu zat kehilangan elektron. Dalam banyak kasus, proses ini melibatkan interaksi dengan oksigen, meskipun oksigen bukan satu-satunya agen oksidasi. Oksidasi seringkali diiringi dengan reaksi reduksi, di mana zat lain menerima elektron yang dilepaskan oleh zat yang teroksidasi. Oleh karena itu, reaksi oksidasi dan reduksi sering disebut sebagai reaksi redoks.
Dalam pembahasan kimia, khususnya saat mempelajari reaksi redoks, ada satu konsep penting yang nggak bisa dilewatkan, yaitu bilangan oksidasi atau sering disingkat biloks. Konsep ini jadi dasar untuk memahami bagaimana elektron berpindah dalam suatu reaksi, serta membantu kita mengidentifikasi perubahan yang terjadi pada suatu unsur. Tanpa memahami biloks, akan sulit untuk menganalisis reaksi kimia secara lebih mendalam.
Pelajari juga mengenai 4 jenis bilangan kuantum beserta studi kasusnya.
Definisi dan Konsep Dasar
Arti oksidasi dalam konteks kimia adalah peningkatan bilangan oksidasi (biloks) suatu atom dalam senyawa atau molekul. Bilangan oksidasi adalah nilai yang menunjukkan jumlah elektron yang hilang atau diperoleh oleh suatu atom dalam proses kimia. Sebagai contoh, ketika besi (Fe) bereaksi dengan oksigen (O2) untuk membentuk besi oksida (Fe2O3), besi mengalami peningkatan bilangan oksidasi dari 0 menjadi +3.
Bilangan oksidasi adalah angka yang menunjukkan jumlah elektron yang dilepas atau diterima oleh suatu atom ketika berikatan dengan atom lain dalam suatu senyawa atau ion. Konsep ini sering muncul saat kamu belajar cara menghitung biloks dalam berbagai senyawa kimia. Jika suatu atom melepaskan elektron, maka biloksnya bernilai positif. Sebaliknya, jika atom menerima elektron, maka biloksnya akan bernilai negatif. Sementara itu, unsur dalam bentuk bebas (tidak berikatan) memiliki biloks nol.
Sementara itu, unsur bebas seperti O₂, H₂, atau Fe dalam bentuk murni selalu memiliki biloks nol. Jadi kalau kamu ditanya unsur bebas apa saja, jawabannya adalah semua unsur yang tidak berikatan dengan unsur lain.
Karbon monoksida (CO), di mana karbon memiliki bilangan oksidasi +2, dikenal sebagai pereduksi kuat karena mudah mengalami oksidasi menjadi karbon dioksida (CO₂) yang lebih stabil dengan biloks +4.
Pentingnya Memahami Biloks dalam Kimia
Memahami bilangan oksidasi punya peran yang sangat penting dalam berbagai aspek kimia. Salah satunya adalah untuk menentukan apakah suatu reaksi termasuk reaksi oksidasi, reduksi, atau keduanya (redoks). Dengan melihat perubahan biloks, kita bisa mengetahui unsur mana yang mengalami kenaikan atau penurunan bilangan oksidasi.
Selain itu, biloks juga sangat membantu dalam:
- Menentukan zat yang bertindak sebagai oksidator dan reduktor
- Menyeimbangkan persamaan reaksi redoks dengan lebih sistematis
- Menganalisis reaksi kimia dalam larutan maupun reaksi kompleks
- Menyelesaikan soal dengan cara menentukan bilangan oksidasi
- Memahami proses kimia dalam kehidupan sehari-hari, seperti korosi, pembakaran, dan reaksi dalam tubuh makhluk hidup
Dengan menguasai konsep bilangan oksidasi, kamu akan lebih mudah memahami berbagai materi kimia lanjutan dan mampu menyelesaikan soal-soal dengan lebih percaya diri.
Aturan Penentuan Bilangan Oksidasi
Setelah memahami konsep dasar, langkah berikutnya adalah memahami aturan bilangan oksidasi. Aturan ini sangat penting karena menjadi dasar dalam proses menentukan biloks suatu unsur dalam senyawa.
Aturan Umum Penentuan Biloks
Berikut adalah aturan-aturan dasar yang paling sering digunakan:
- Unsur bebas memiliki biloks = 0
Semua unsur yang tidak berikatan dengan unsur lain, baik dalam bentuk atom (seperti Fe, Cu, Na) maupun molekul unsur (seperti H₂, O₂, Cl₂), selalu bernilai nol. - Biloks ion sama dengan muatannya
Untuk ion monoatom (satu atom), biloksnya langsung mengikuti muatan ion.
Contoh: Na⁺ = +1, Mg²⁺ = +2, Al³⁺ = +3, sehingga sering muncul juga istilah seperti biloks mg dalam soal.
Sedangkan untuk ion poliatom, jumlah seluruh biloks unsur penyusunnya harus sama dengan total muatan ion.
Contoh: SO₄²⁻ memiliki total biloks -2. - Logam golongan utama memiliki biloks tetap
Unsur-unsur tertentu memiliki biloks yang hampir selalu sama:- Golongan IA (alkali) = +1
- Golongan IIA (alkali tanah) = +2
- Golongan IIIA = +3
Ini sering dijadikan “starting point” saat menentukan biloks dalam suatu senyawa.
- Jumlah biloks dalam senyawa netral = 0
Ini adalah dasar dalam cara menghitung biloks pada senyawa. Semua biloks unsur dalam satu senyawa harus jika dijumlahkan menghasilkan nol.
Contoh: H₂O → H = +1 (2 atom = +2), maka O = -2 agar total = 0. - Jumlah biloks dalam ion = total muatan ion
Berbeda dengan senyawa netral, pada ion jumlah biloks harus sama dengan muatannya.
Contoh: NH₄⁺ → total biloks = +1.
Aturan-aturan ini biasanya digunakan secara bersamaan saat melakukan proses penentuan biloks. Jika satu nilai sudah diketahui, kamu bisa mencari biloks unsur lain dengan memanfaatkan keseimbangan jumlah totalnya.
Meskipun ada aturan baku untuk menentukan bilangan oksidasi (biloks), beberapa senyawa memiliki pengecualian yang perlu diingat. Berikut adalah beberapa pengecualian penting:
Pengecualian dalam Aturan Biloks
Walaupun aturan umum cukup membantu, ada beberapa kondisi khusus yang sering jadi “jebakan” kalau tidak diperhatikan:
- Unsur transisi memiliki biloks bervariasi
Logam transisi (golongan B) tidak memiliki satu nilai tetap.
Contohnya:- Cu bisa +1 atau +2
- Fe bisa +2 atau +3
- Au bisa +1 (biloks ag) atau +3
Jadi, kamu harus melihat konteks senyawanya untuk menentukan nilai yang benar.
- Hidrogen bisa bernilai +1 atau -1
- Jika berikatan dengan non-logam (seperti O, Cl), maka H = +1
- Jika berikatan dengan logam (seperti Na, Ca), maka H = -1
Contoh:
H₂O → H = +1
NaH → H = -1
- Oksigen umumnya -2, tapi tidak selalu
- Dalam senyawa biasa → O = -2
- Dalam senyawa peroksida (seperti H₂O₂, BaO₂) → O = -1
Pengecualian ini penting banget karena sering muncul dalam soal dan bisa mengubah hasil akhir secara signifikan.

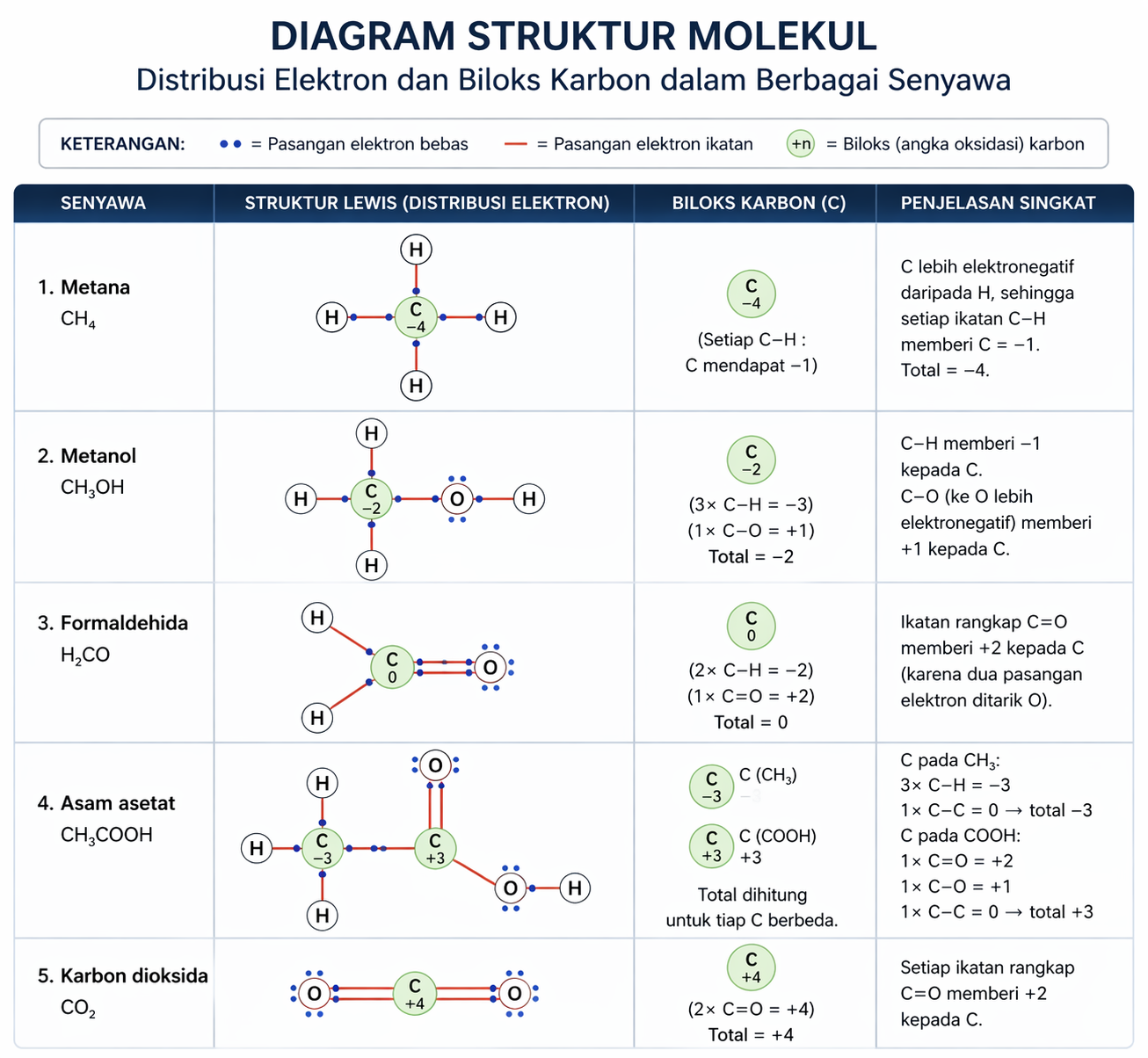
Bilangan Oksidasi Karbon dalam Berbagai Senyawa

Karbon termasuk unsur yang unik karena memiliki rentang bilangan oksidasi yang sangat luas, yaitu dari -4 hingga +4. Variasi ini terjadi karena karbon dapat berikatan dengan berbagai jenis unsur, baik yang bersifat lebih elektropositif seperti hidrogen maupun yang lebih elektronegatif seperti oksigen. Akibatnya, nilai biloks karbon bisa berubah-ubah tergantung lingkungan ikatannya.
Biloks Karbon dalam Senyawa Organik
Dalam senyawa organik, karbon umumnya berikatan dengan hidrogen, oksigen, atau sesama karbon. Nilai biloksnya sangat dipengaruhi oleh jenis ikatan tersebut:
- -4 → Metana (CH₄), karbon hanya berikatan dengan hidrogen
- -2 → Metanol (CH₃OH)
- -1 → Metanal (CH₂O)
- 0 → Etilena (C₂H₄)
Semakin banyak karbon berikatan dengan hidrogen, biloksnya cenderung semakin negatif. Sebaliknya, jika mulai berikatan dengan oksigen, nilainya akan meningkat (lebih positif). Fenomena ini sering muncul dalam soal biloks n dan karbon karena keduanya sama-sama memiliki variasi biloks yang luas.
Contoh menarik ada pada senyawa seperti asam asetat (CH₃COOH), di mana terdapat dua atom karbon dengan biloks berbeda:
- Karbon pada gugus CH₃ = -3
- Karbon pada gugus COOH = +3
Ini menunjukkan bahwa dalam satu molekul organik, nilai biloks karbon bisa tidak sama.
Biloks Karbon dalam Senyawa Anorganik
Pada senyawa anorganik, karbon biasanya berikatan dengan oksigen atau unsur lain yang lebih elektronegatif, sehingga biloksnya cenderung positif:
- +2 → Karbon monoksida (CO)
- +3 → Asam format (HCOOH), ion oksalat (C₂O₄²⁻)
- +4 → Karbon dioksida (CO₂), kalsium karbonat (CaCO₃)
Semakin banyak ikatan karbon dengan oksigen, biloksnya akan semakin besar (lebih positif). Misalnya, pada CO₂, karbon mencapai biloks maksimum yaitu +4.
Dengan memahami pola ini, kamu bisa lebih cepat dalam proses cara menentukan bilangan oksidasi tanpa harus menghitung dari awal.
Contoh Reaksi Oksidasi: Menjelajahi Berbagai Proses Kimia
Reaksi oksidasi adalah salah satu jenis reaksi kimia yang sangat penting dalam berbagai aspek kehidupan sehari-hari dan aplikasi industri. Di bawah ini, kita akan membahas beberapa contoh reaksi oksidasi yang signifikan, menjelaskan mekanisme yang mendasarinya, dan pentingnya dalam konteks praktis.
- Pembakaran Hidrokarbon
Pembakaran hidrokarbon adalah salah satu contoh reaksi oksidasi yang paling umum. Hidrokarbon seperti metana (CH4), propana (C3H8), dan butana (C4H10) bereaksi dengan oksigen untuk menghasilkan karbon dioksida dan air, serta melepaskan energi dalam bentuk panas dan cahaya.
Contoh Reaksi:
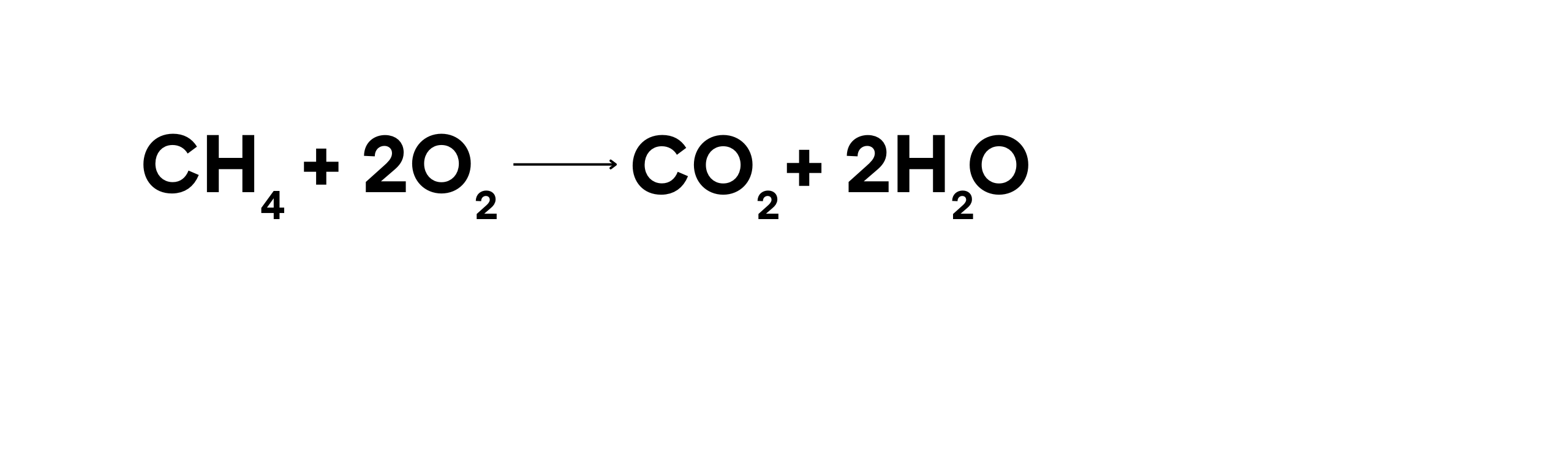
Dalam reaksi ini:
- Metana (CH4) teroksidasi menjadi karbon dioksida (CO2).
- Oksigen (O2) bertindak sebagai agen pengoksidasi.
Proses ini sangat penting dalam penggunaan bahan bakar untuk pemanas, memasak, dan sebagai sumber energi dalam mesin pembakaran internal.
- Respirasi Seluler
Respirasi seluler adalah proses biologis di mana glukosa (C6H12O6) dioksidasi untuk menghasilkan energi yang diperlukan oleh sel-sel organisme hidup. Reaksi ini terjadi di dalam mitokondria sel dan menghasilkan karbon dioksida dan air sebagai produk samping.
Contoh Reaksi:
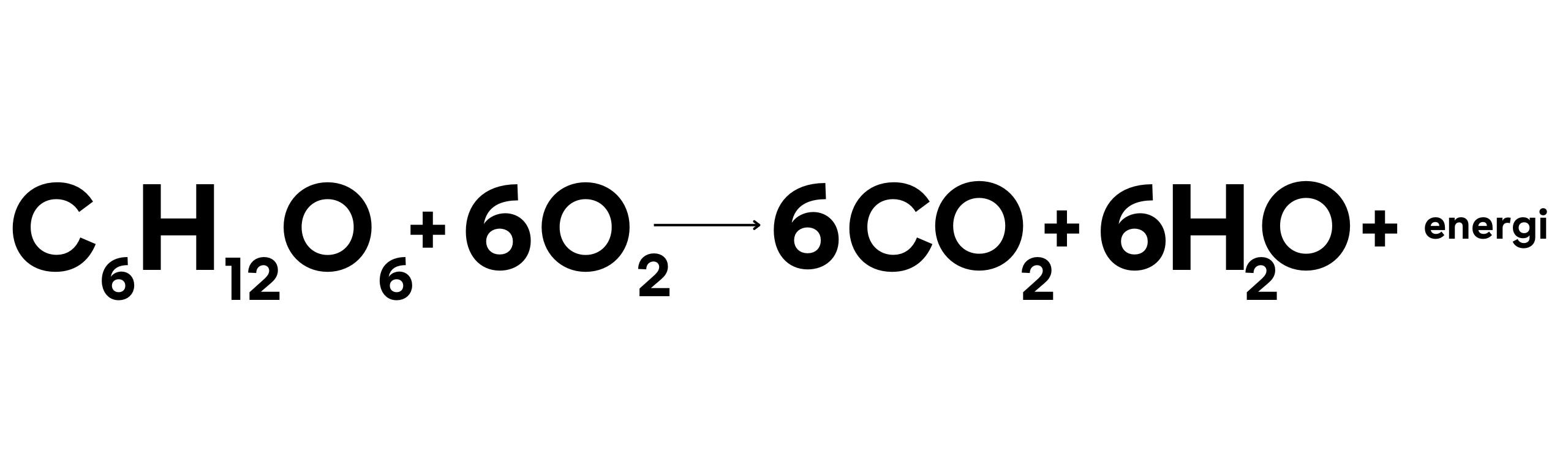
Dalam reaksi ini:
- Glukosa teroksidasi menjadi karbon dioksida.
- Oksigen tereduksi menjadi air.
Energi yang dihasilkan dari proses ini digunakan oleh sel untuk melakukan berbagai fungsi vital.
- Perkaratan Besi
Perkaratan besi adalah contoh reaksi oksidasi yang terjadi ketika besi (Fe) bereaksi dengan oksigen (O2) dan air (H2O) untuk membentuk besi oksida (Fe2O3), yang dikenal sebagai karat. Dalam proses ini, muatan Fe berubah dari 0 menjadi +3. Hal ini mengindikasikan bahwa besi mengalami oksidasi, yaitu kehilangan elektron.
Contoh Reaksi:
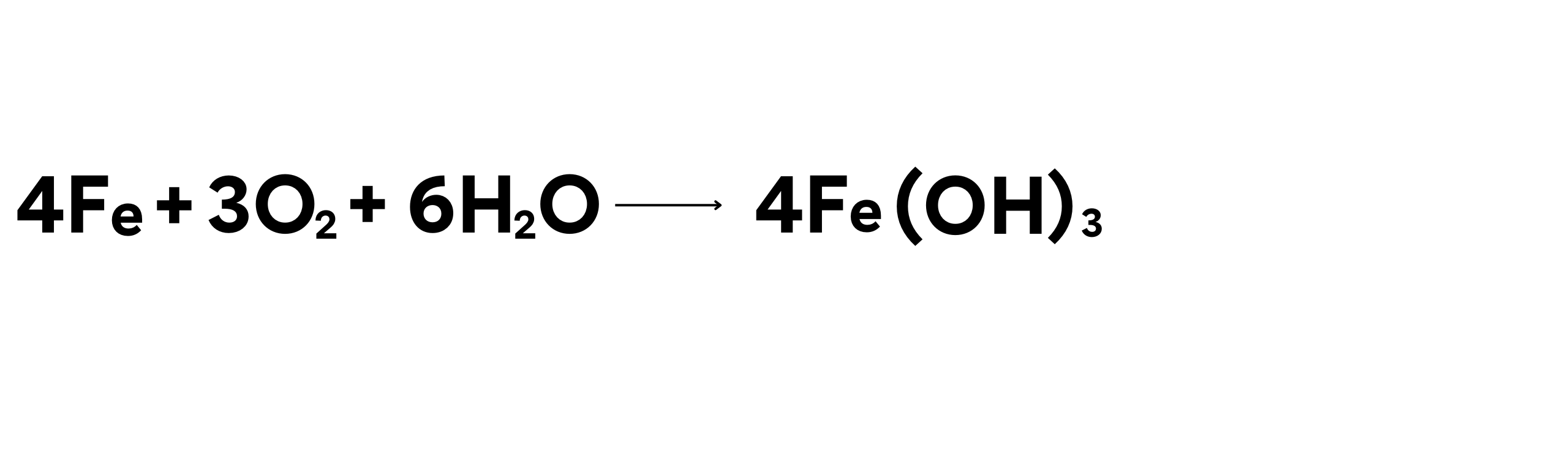
Dalam reaksi ini:
- Besi teroksidasi menjadi besi hidroksida, yang kemudian mengoksidasi lebih lanjut menjadi besi oksida (karat).
Proses perkaratan ini menyebabkan kerugian ekonomi yang signifikan dalam perawatan dan penggantian infrastruktur logam.
- Oksidasi Alkohol
Oksidasi alkohol adalah proses di mana alkohol diubah menjadi aldehida atau keton, dan selanjutnya dapat dioksidasi menjadi asam karboksilat. Proses ini penting dalam kimia organik dan industri kimia.
Contoh Reaksi (oksidasi etanol menjadi asetaldehida):
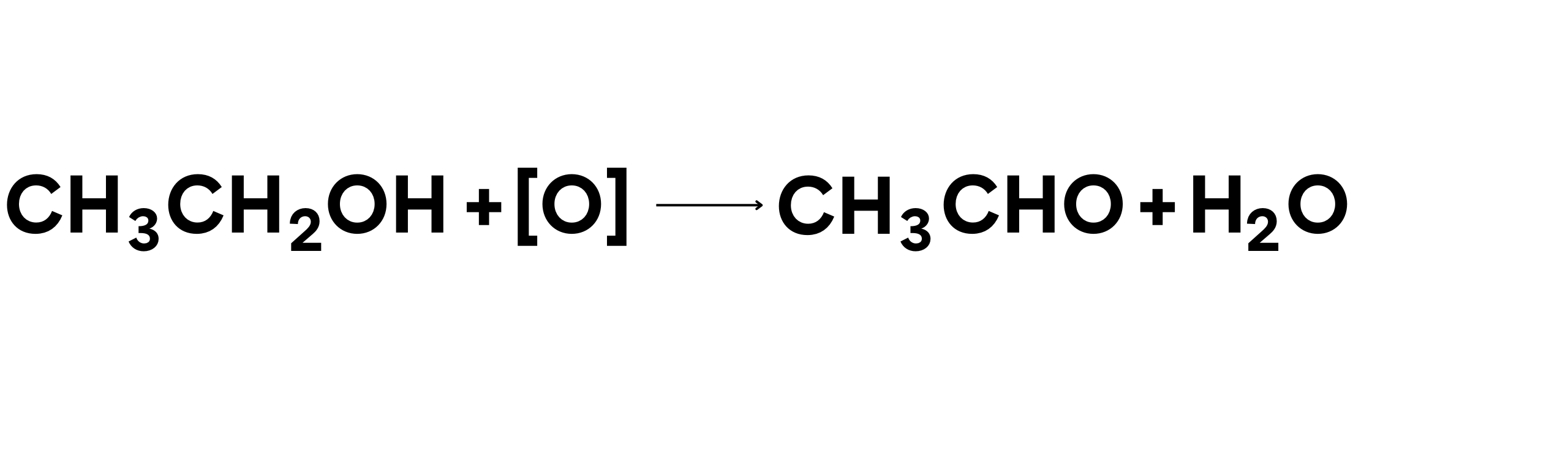
Dalam reaksi ini:
- Etanol (CH3CH2OH) teroksidasi menjadi asetaldehida (CH3CHO).
- Produksi Asam Sulfat
Produksi asam sulfat (H2SO4) melalui proses kontak adalah contoh penting dari reaksi oksidasi dalam industri kimia. Dalam proses ini, belerang dioksida (SO2) dioksidasi menjadi belerang trioksida (SO3), yang kemudian bereaksi dengan air untuk membentuk asam sulfat.
Contoh Reaksi:
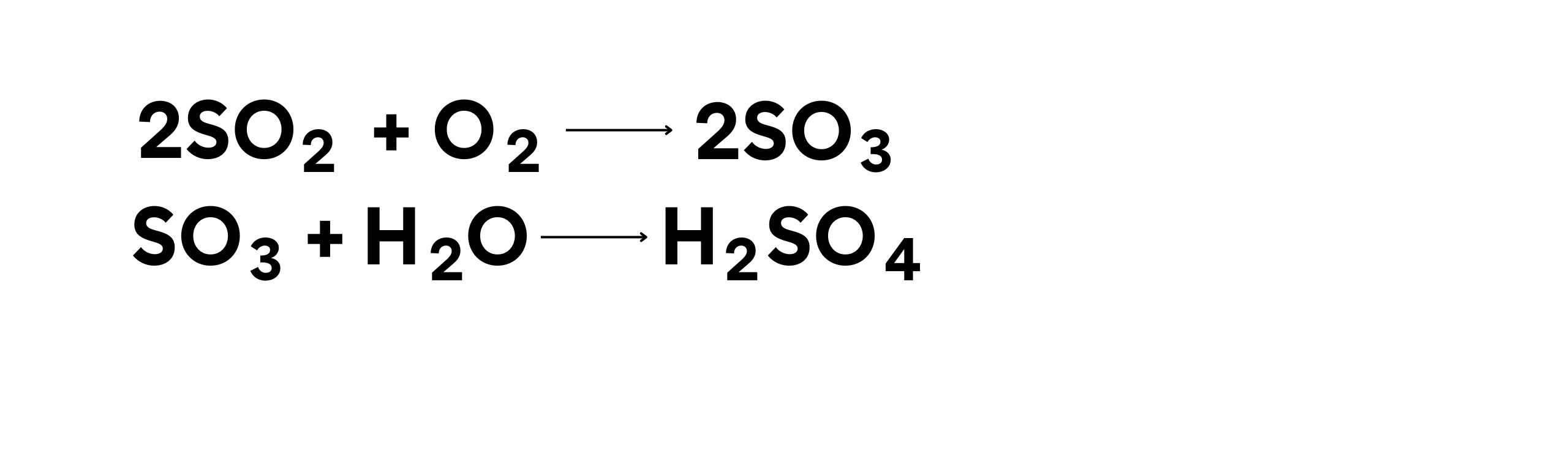
Dalam reaksi ini:
- Belerang dioksida (SO2) teroksidasi menjadi belerang trioksida (SO3).
Proses ini sangat penting dalam produksi asam sulfat, yang merupakan salah satu bahan kimia industri paling banyak digunakan.
- Fotosintesis (Tahap Oksidasi Air)
Fotosintesis adalah proses di mana tumbuhan hijau, alga, dan beberapa bakteri menggunakan energi matahari untuk mengubah karbon dioksida dan air menjadi glukosa dan oksigen. Tahap awal fotosintesis melibatkan oksidasi air untuk menghasilkan oksigen.
Contoh Reaksi:
Dalam reaksi ini:
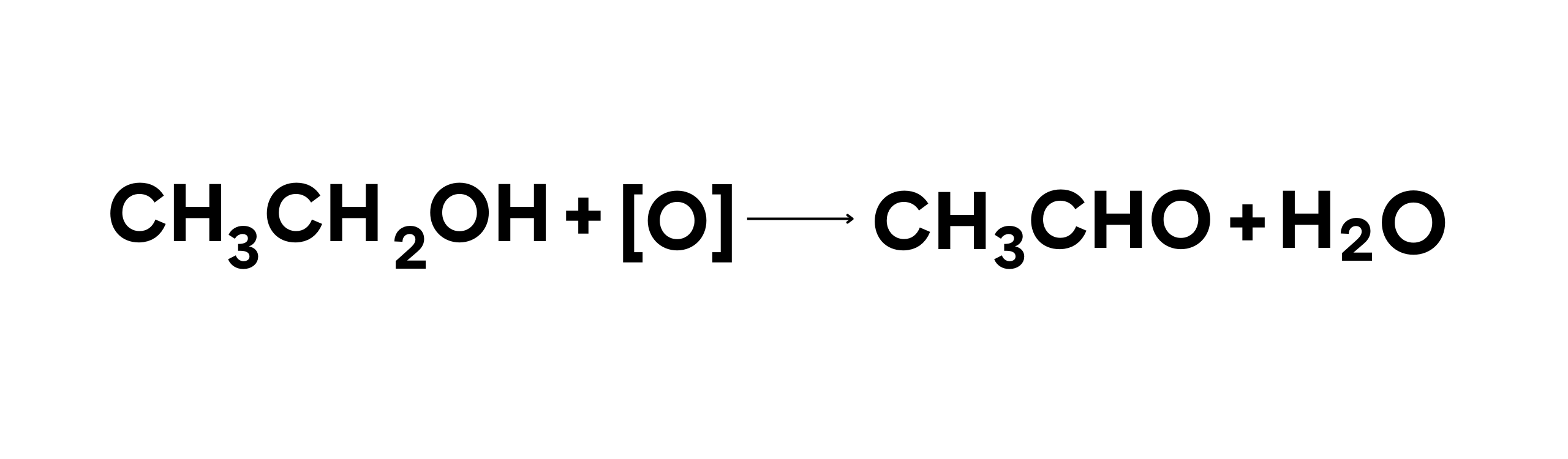
Air (H2O) teroksidasi menjadi oksigen (O2).Tahap ini sangat penting karena menyediakan elektron yang diperlukan untuk tahap selanjutnya dalam proses fotosintesis, serta menghasilkan oksigen yang esensial bagi kehidupan aerobik di Bumi.
Contoh Soal Reaksi Redoks (Oksidasi)
Berikut adalah beberapa contoh soal reaksi redoks yang dapat membantu Anda memahami bagaimana bilangan oksidasi berubah dalam suatu reaksi kimia. Dalam reaksi redoks, selalu ada dua proses yang terjadi bersamaan, yaitu oksidasi (peningkatan biloks) dan reduksi (penurunan biloks).
Contoh 1: Reaksi Redoks Pembakaran Metana
Reaksi pembakaran metana (CH₄) adalah contoh reaksi redoks, di mana metana teroksidasi, dan oksigen tereduksi. Berikut adalah contoh soal untuk reaksi ini:
Tuliskan reaksi redoks antara metana (CH₄) dan oksigen (O₂), dan tentukan perubahan bilangan oksidasi dari unsur yang terlibat.
Jawaban:
- CH₄ + 2O₂ → CO₂ + 2H₂O
- Dalam reaksi ini, karbon (C) mengalami peningkatan biloks dari -4 menjadi +4 (oksidasi), sedangkan oksigen (O₂) mengalami penurunan biloks dari 0 menjadi -2 (reduksi).
Contoh 2: Reaksi Redoks pada Proses Perkaratan Besi
Perkaratan besi adalah reaksi redoks yang sangat umum. Dalam proses ini, besi (Fe) teroksidasi, sedangkan oksigen (O₂) tereduksi.
Tuliskan reaksi redoks untuk perkaratan besi dan tentukan perubahan bilangan oksidasi dari unsur-unsur yang terlibat.
Jawaban:
- 3Fe + 4O₂ → 2Fe₂O₃
Dalam reaksi ini, besi (Fe) mengalami peningkatan biloks dari 0 menjadi +3 (oksidasi), sedangkan oksigen (O₂) mengalami penurunan biloks dari 0 menjadi -2 (reduksi).
Lanjutkan membaca artikel Superprof ini untuk memahami bentuk-bentuk bilangan kuantum beserta contohnya!
Cara Menentukan Bilangan Oksidasi Karbon
Menentukan bilangan oksidasi (biloks) karbon sebenarnya tidak sesulit yang dibayangkan, asalkan kamu paham pola dan aturan dasarnya. Kuncinya ada pada keseimbangan total biloks dalam suatu senyawa serta memahami kecenderungan karbon saat berikatan dengan unsur lain seperti hidrogen dan oksigen.
Langkah-langkah Penentuan Biloks C
Berikut langkah sistematis yang bisa kamu ikuti:
- Tentukan jenis senyawa (netral atau ion)
Jika senyawa netral, total biloks = 0. Jika ion, total biloks = sesuai muatan ion. - Tentukan biloks unsur lain yang sudah pasti
Umumnya:- H = +1 (kecuali pada hidrida logam = -1)
- O = -2 (kecuali pada peroksida = -1)
- Gunakan persamaan jumlah biloks
Jumlahkan semua biloks dalam senyawa, lalu samakan dengan total (0 untuk senyawa netral). Ini adalah inti dari cara menghitung biloks. - Hitung biloks karbon (C)
Jadikan biloks karbon sebagai variabel, lalu selesaikan persamaan. - Perhatikan jenis ikatan (opsional untuk organik)
- Ikatan C–H → membuat C lebih negatif
- Ikatan C–O → membuat C lebih positif
- Ikatan C–C → tidak berpengaruh
Langkah ini membantu kamu memperkirakan nilai biloks dengan cepat, terutama pada senyawa organik.
Contoh Soal dan Pembahasan
Berikut beberapa contoh soalbiloks yang sering muncul:
1. Tentukan biloks C dalam CO₂
- O = -2, jumlah O = 2 → total = -4
- Total senyawa = 0
- Maka: C + (-4) = 0 → C = +4
2. Tentukan biloks C dalam CH₄
- H = +1, jumlah H = 4 → total = +4
- Total senyawa = 0
- Maka: C + 4 = 0 → C = -4
3. Tentukan biloks C dalam CH₃OH (metanol)
- H = +1 (4 atom total, termasuk di OH) → +4
- O = -2
- Total = 0
- Maka: C + 4 - 2 = 0 → C = -2
4. Tentukan biloks C dalam HCOOH (asam format)
- H = +1 (2 atom) → +2
- O = -2 (2 atom) → -4
- Total = 0
- Maka: C + 2 - 4 = 0 → C = +2
Latihan seperti ini penting untuk membiasakan diri dalam proses menentukan biloks dengan cepat dan akurat.
Tabel Bilangan Oksidasi Unsur Umum
Dalam praktiknya, ada sejumlah bilangan oksidasi unsur yang sering muncul dan dijadikan acuan. Nilai-nilai ini berasal dari kecenderungan unsur dalam sistem periodik dan aturan dasar kimia. Biasanya ini dirangkum dalam bentuk tabel biloks agar lebih mudah dipahami.
Biloks Unsur Golongan Utama
Unsur golongan utama (golongan A) umumnya memiliki bilangan oksidasi yang relatif tetap atau mengikuti pola tertentu:
| Golongan | Unsur | Bilangan Oksidasi Umum |
|---|---|---|
| IA | H (Hidrogen) | +1 (dengan nonlogam), -1 (dengan logam) |
| Li, Na, K, Rb, Cs, Fr | +1 | |
| IIA | Be, Mg, Ca, Sr, Ba | +2 |
| IIIA | Al, Ga | +3 |
| IVA | C (Karbon) | -4, +2, +4 |
| Si, Ge, Sn, Pb | +2, +4 | |
| VA | N (Nitrogen) | -3, +2, +3, +4, +5 |
| P (Fosfor) | -3, +3, +5 | |
| VIA | O (Oksigen) | -2 (umum), -1 (peroksida), +2 (dengan F) |
| S (Sulfur) | -2, +4, +6 | |
| VIIA | F (Fluorin) | -1 (selalu) |
| Cl, Br, I | -1, +1, +3, +5, +7 |
Memahami pola ini akan sangat membantu dalam proses cara menentukan bilangan oksidasi secara cepat.
Biloks Unsur Transisi
Unsur transisi (golongan B) dikenal memiliki bilangan oksidasi yang bervariasi. Hal ini terjadi karena elektron pada subkulit d dapat terlibat dalam pembentukan ikatan, sehingga memungkinkan satu unsur memiliki lebih dari satu nilai biloks tergantung pada senyawanya.
Berikut beberapa contoh biloks unsur transisi yang sering ditemui:
| Unsur | Bilangan Oksidasi Umum |
|---|---|
| Fe (Besi) | +2, +3 |
| Cu (Tembaga) | +1, +2 |
| Zn (Seng) | +2 |
| Ag (Perak) | +1 |
| Au (Emas) | +1, +3 |
- Besi (Fe) sering ditemukan dalam dua bentuk, yaitu Fe²⁺ dan Fe³⁺
- Tembaga (Cu) bisa bernilai +1 atau +2 tergantung senyawanya
- Seng (Zn) cenderung stabil di biloks +2
- Perak (Ag) umumnya hanya memiliki biloks +1
- Emas (Au) dapat memiliki biloks +1 dan +3
Karena sifatnya yang tidak tetap, penentuan biloks unsur transisi biasanya perlu dianalisis berdasarkan senyawa yang dibentuk, tidak bisa hanya mengandalkan hafalan seperti pada golongan utama.
Contoh lain yang sering muncul adalah biloks ag yang umumnya +1. Karena variasinya banyak, unsur transisi tidak bisa hanya dihafal, tapi harus dipahami dari konteks senyawanya.
Untuk cek seberapa paham kamu dalam mempelajari Biloks, perhatikan contoh soal dibawah ini :
| Soal | Pembahasan |
| Tentukan biloks C dalam CO₂ | O = -2, jumlah O = 2 Total = -4 Karena senyawa netral, total = 0. Maka: C + (-4) = 0 C = +4 |
| Tentukan biloks C dalam CH₄ | H = +1 Jumlah H = 4 Total = +4 Total senyawa = 0 Maka: C + 4 = 0 C = -4 |
| Tentukan biloks C dalam CH₃OH | H = +1 (4 atom) +4, O = -2 Total = 0 Maka: C + 4 - 2 = 0 C = -2 |
Dengan memahami biloks dan aturan-aturan yang menyertainya, kamu bisa lebih mudah menentukan bilangan oksidasi dalam berbagai senyawa. Jangan lupa, rumus redoks juga terlibat dalam perubahan biloks yang terjadi selama reaksi. Jika anda merasa kesulitan memahami biloks, jangan ragu untuk mencari les privat di Superprof! Temukan guru kimia terbaik di sekitar anda yang siap membantu menjelaskan materi biloks dan reaksi redoks dengan cara yang mudah dipahami.
Selain itu, Superprof punya artikel lain tentang konfigurasi elektron dan diagram orbital yang bisa membantu Anda memahami subjek kimia lebih jauh!
Ringkaskan dengan AI















Agar tali silaturahmi tidak terputus,adakah seratus min
haha belum ada nih, coba pinjem sama yang lain