Yang jarang disadari, kimia sangat dekat dengan hal-hal di sekitar kita. Apakah Anda pernah mengamati petani saat memupuk tanamannya? Atau Anda juga pernah melakukannya sendiri? Saat memupuk tanaman, bagian terpenting adalah konsentrasi pengenceran pupuk yang harus disesuaikan dengan perbandingan tertentu. Tidak boleh terlalu pekat maupun terlalu encer. Hal itu dapat berdampak pada metabolise di dalam tubuh tanaman. Dalam memastikan komposisi unsur kimia yang cocok untuk pupuk, disitulah perhitungan stokiometri bekerja.
Tapi, apa itu stokiometri? Dan bagaimana hal itu digunakan?
Panduan kami akan memberi rangkuman stokiometri yang secara singkat dan padat akan menjelaskan pada Anda materi tentang stokiometri beserta rumus stokiometri.
Stokiometri merupakan mata pelajaran wajib kimia kelas 10. Materi kimia stokiometri ini selalu muncul dalam tes UTBK SBMPTN, maka dari itu Anda perlu banyak berlatih tentang soal stokiometri.
Kami akan membantu Anda belajar kimia dengan mudah dan memberikan pemaparan yang cepat untuk Anda pahami. Jika Anda merasa kesulitan, kursus privat adalah solusi yang bagus untuk mendukung kemajuan Anda.

Pengantar Rumus Molekul dan Rumus Empiris
Sebagai bahan pengantar materi stokiometri, Anda perlu memahami terlebih dahulu konsep rumus molekul dan rumus empiris.

Pupuk yang sering digunakan adalah jenis pupuk urea. Pupuk urea memiliki rumus molekul CH4N2O. Rumus molekul merupakan rumus yang menunjukkan jumlah atom setiap unsur dalam suatu senyawa dan digunakan sebagai lambang suatu senyawa. Semetara, rumus empiris merupakan rumus yang memiliki perbandingan atom-atom paling sederhana dalam suatu senyawa.
Untuk menentukan rumus empiris, ada dua hal yang dapat kita lakukan. Pertama, rumus empiris didapatkan dengan menyederhanakan jumlah atom penyusun rumus molekul agar diperoleh bilangan bulat paling kecil. Atau kedua, rumus empiris juga dapat ditentukan melalui perbandingan mol unsur-unsur penyusun senyawa dengan syarat massanya diketahui. Contoh untuk menentukan rumus empiris dari senyawa C6H12O6 dapat dilakukan dengan cara pertama. Dari penyederhanaan rumus molekul, didapatkan (CH2O)6 sehingga rumus empiris dari C6H12O6 adalah CH2O.
Di satu sisi, beberapa senyawa memiliki rumus molekul yang sama dengan rumus empirisnya dan beberapa berbeda. Untuk menentukan rumus molekul, gunakan persamaan berikut;
Mr RUMUS EMPIRIS x n = Mr RUMUS MOLEKUL
(RUMUS EMPIRIS)n = RUMUS MOLEKUL
Dengan keterangan, n merupakan kelipatan rumus empiris terhadap rumus molekul.
Untuk membantu Anda lebih memiliki konsep ini, kami menyediakan satu latihan soal. Pastikan untuk Anda mencobanya terlebih dahulu sebelum melihat kunci jawaban. Berlatih soal-soal kimia membantu Anda belajar kimia dengan mudah.
Contoh Soal:
Suatu senyawa memiliki rumus empiris CH2O. Jika Mr senyawa tersebut adalah 150, tentukan rumus molekul senyawanya! (Ar H = 1, C = 12, dan O = 16)
Pembahasan:
Untuk menjawab soal tersebut, tentukan terlebih dahulu massa molekul relatifnya (Mr)!
Mr CH2O = (1 x Ar C) + (2 x Ar H) + (1 x Ar O)
= (1x12) + (2x1) + (1x16) = 30
Setelah itu, tentukan nilai n melalui persamaan
Mr RUMUS EMPIRIS x n = Mr RUMUS MOLEKUL
(RUMUS EMPIRIS)n = RUMUS MOLEKUL
Maka, Mr rumus empiris = Mr rumus molekul
30 x n = 150
n = 5
Dengan n = 5, didapatkan:
Rumus molekul = (Rumus empiris)n
= (CH2O)5 = C5H10O5
Bagaimana, kimia mudah bukan?
Sekarang, coba asah kemampuan Anda dengan mengerjakan latihan soal berikut ini:
Diketahui sebuah persamaan reaksi kimia: 2SO2 (g) + O2 (g) → 2SO3 (g). Tentukan massa molekul relatif gas O2 dan SO2.
Pengertian Stoikiometri
Secara sederhana, stoikiometri berasal dari bahasa Yunani, "stoicheion" yang berarti unsur, dan "metron" yang berarti pengukuran. Jadi, stoikiometri adalah ilmu kimia yang mempelajari tentang hubungan kuantitatif antara zat-zat yang terlibat dalam reaksi kimia, baik itu reaktan maupun produk.
Melalui stoikiometri, kita dapat menentukan berapa banyak reaktan yang dibutuhkan atau berapa banyak produk yang dihasilkan dalam suatu reaksi kimia. Hubungan kuantitatif ini didasarkan pada hukum-hukum dasar kimia, seperti hukum kekekalan massa, yang menyatakan bahwa massa total zat sebelum dan sesudah reaksi akan tetap sama.

Hukum-Hukum Dasar dalam Stoikiometri
Dalam stoikiometri, terdapat beberapa hukum dasar yang menjadi landasan untuk melakukan perhitungan kuantitatif zat-zat yang terlibat dalam reaksi kimia. Hukum-hukum ini menjelaskan hubungan antara massa, jumlah zat, dan volume zat yang berpartisipasi dalam reaksi kimia. Berikut adalah hukum-hukum dasar yang penting dalam stoikiometri:
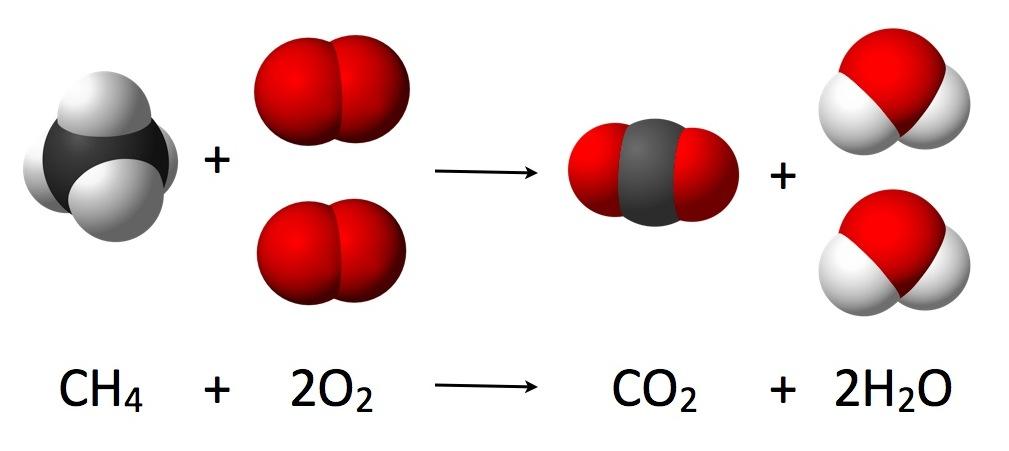
1. Hukum Kekekalan Massa (Hukum Lavoisier)
Hukum Kekekalan Massa, yang juga dikenal sebagai Hukum Lavoisier, diperkenalkan oleh Antoine Lavoisier pada akhir abad ke-18. Hukum ini menyatakan bahwa:
"Massa total zat sebelum reaksi kimia sama dengan massa total zat setelah reaksi."
Artinya, dalam suatu reaksi kimia, jumlah massa reaktan yang digunakan akan sama dengan massa produk yang dihasilkan. Zat-zat tidak hilang atau tercipta dalam proses reaksi kimia, melainkan berubah bentuk atau berikatan dengan unsur lain untuk membentuk zat baru.
2. Hukum Perbandingan Tetap (Hukum Proust)
Hukum Perbandingan Tetap, yang dikemukakan oleh Joseph Proust pada tahun 1799, menyatakan bahwa:
"Setiap senyawa kimia selalu mengandung unsur-unsur dengan perbandingan massa yang tetap dan spesifik."
Dengan kata lain, dalam senyawa tertentu, unsur-unsur penyusunnya akan selalu terdapat dalam perbandingan massa yang sama, tidak peduli berapa banyak atau sedikit jumlah senyawa tersebut. Hukum ini menunjukkan konsistensi komposisi dalam pembentukan senyawa.
3. Hukum Perbandingan Berganda (Hukum Dalton)
Hukum Perbandingan Berganda, yang ditemukan oleh John Dalton pada tahun 1803, menyatakan bahwa:
"Jika dua unsur dapat membentuk lebih dari satu senyawa, maka perbandingan massa salah satu unsur yang bersenyawa dengan massa unsur lainnya dalam senyawa-senyawa tersebut adalah bilangan bulat sederhana."
Hukum ini berlaku ketika dua unsur yang sama membentuk lebih dari satu jenis senyawa. Perbandingan massa antara unsur-unsur dalam senyawa-senyawa tersebut akan mengikuti rasio bilangan bulat sederhana.
4. Hukum Perbandingan Volume (Hukum Gay-Lussac)
Hukum Perbandingan Volume, yang ditemukan oleh Joseph Gay-Lussac pada tahun 1808, menyatakan bahwa:
"Pada suhu dan tekanan yang sama, volume gas-gas yang bereaksi dan gas yang dihasilkan dalam suatu reaksi kimia akan memiliki perbandingan bilangan bulat yang sederhana."
Hukum ini mengacu pada reaksi-reaksi yang melibatkan gas, dan menyatakan bahwa perbandingan volume gas yang bereaksi sebanding dengan jumlah mol gas dalam reaksi kimia tersebut.
5. Hipotesis Avogadro
Hipotesis Avogadro, yang dikemukakan oleh Amedeo Avogadro pada tahun 1811, menyatakan bahwa:
"Pada suhu dan tekanan yang sama, volume gas yang sama akan mengandung jumlah molekul yang sama."
Dengan kata lain, jumlah molekul dalam volume gas yang sama tidak bergantung pada jenis gas tersebut, asalkan gas tersebut berada pada suhu dan tekanan yang sama. Hipotesis ini kemudian melahirkan konsep mol dan Tetapan Avogadro (6,02 x 10²³ partikel/mol).

Jenis-Jenis Stoikiometri
Stoikiometri adalah ilmu yang mempelajari hubungan kuantitatif antara reaktan dan produk dalam reaksi kimia. Dengan memahami stoikiometri, kita dapat menghitung jumlah zat yang diperlukan dalam suatu reaksi atau jumlah produk yang dihasilkan. Dalam kimia, terdapat beberapa jenis stoikiometri yang perlu dipahami untuk dapat melakukan perhitungan dengan tepat. Berikut adalah penjelasan mengenai jenis-jenis stoikiometri:
1. Stoikiometri Reaksi
Stoikiometri reaksi adalah jenis stoikiometri yang paling umum digunakan. Stoikiometri ini mempelajari hubungan kuantitatif antara zat-zat yang berpartisipasi dalam reaksi kimia. Dalam stoikiometri reaksi, kita dapat menghitung berapa banyak reaktan yang dibutuhkan untuk menghasilkan produk tertentu, atau sebaliknya, berapa banyak produk yang dihasilkan dari sejumlah reaktan.
Stoikiometri reaksi membantu dalam menyetarakan persamaan kimia sehingga jumlah atom setiap unsur di sisi reaktan sama dengan di sisi produk. Koefisien dalam persamaan kimia menunjukkan jumlah mol dari masing-masing zat yang berpartisipasi dalam reaksi. Ini memungkinkan kita untuk melakukan perhitungan stoikiometri yang melibatkan perbandingan mol.
2. Stoikiometri Komposisi
Stoikiometri komposisi mempelajari hubungan kuantitatif antara unsur-unsur yang ada dalam suatu senyawa. Dengan stoikiometri ini, kita dapat menentukan berapa banyak atom atau massa masing-masing unsur yang terkandung dalam suatu senyawa.
Stoikiometri komposisi sering digunakan untuk menghitung rumus empiris dan rumus molekul suatu senyawa. Rumus empiris adalah rumus kimia yang menunjukkan perbandingan paling sederhana antara jumlah atom unsur-unsur dalam senyawa. Sementara itu, rumus molekul menunjukkan jumlah atom sebenarnya dari unsur-unsur tersebut dalam senyawa.
3. Stoikiometri Gas
Stoikiometri gas adalah jenis stoikiometri yang berhubungan dengan reaksi kimia yang melibatkan gas. Dalam stoikiometri ini, kita menggunakan hukum gas ideal untuk menghitung volume, tekanan, atau suhu gas yang terlibat dalam reaksi kimia. Persamaan gas ideal, yang dinyatakan dengan rumus:
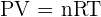
di mana:
- P = tekanan gas (atm),
- V = volume gas (liter),
- n = jumlah mol gas,
- R = tetapan gas (0,0821 L atm/mol K),
- T = suhu gas (Kelvin).
Stoikiometri gas sering digunakan dalam kondisi STP (Standard Temperature and Pressure), di mana pada kondisi STP (suhu 0°C dan tekanan 1 atm), 1 mol gas ideal menempati volume 22,4 liter.
Daftar Istilah Penting!
Ada beberapa istilah yang perlu diperhatikan dalam materi stokiometri:
Massa Atom Relatif (Ar)
Massa atom relatif merupakan perbandingan massa suatu atom dengan 1/12 kali massa suatu atom isotop karbon-12 atau C-12.
Massa Molekul Relatif (Mr)
Massa molekul relatif digunakan untuk mencari perbandingan massa satu molekul senyawa dengan 1/12 kali massa satu atom isotop karbon-12 atau C-12.
Stoikiometri Larutan
Stoikiometri larutan adalah jenis stoikiometri yang berfokus pada reaksi kimia yang terjadi dalam larutan. Dalam stoikiometri ini, molaritas (M), yang merupakan konsentrasi larutan, menjadi faktor penting. Molaritas didefinisikan sebagai jumlah mol zat terlarut dalam setiap liter larutan, yang dirumuskan sebagai:
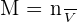
di mana:
- M = molaritas (mol/L),
- n = jumlah mol zat terlarut,
- V = volume larutan (liter).
Dalam stoikiometri larutan, kita sering melakukan perhitungan untuk menentukan konsentrasi larutan, jumlah mol zat terlarut, atau volume larutan yang diperlukan dalam suatu reaksi.
Stoikiometri Konsep Mol
Salah satu konsep paling mendasar dalam stoikiometri adalah konsep mol. Mol adalah satuan yang digunakan untuk menyatakan jumlah zat berdasarkan jumlah partikel, seperti atom, molekul, atau ion. Satu mol zat mengandung 6,02 x 10²³ partikel, yang dikenal sebagai tetapan Avogadro.
Stoikiometri konsep mol memungkinkan kita untuk melakukan hitungan kimia dengan mudah, karena kita dapat mengonversi antara massa zat, jumlah mol, dan jumlah partikel menggunakan persamaan mol:
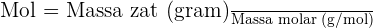
Dengan menggunakan stoikiometri konsep mol, kita dapat memprediksi berapa banyak zat yang akan bereaksi atau dihasilkan dalam suatu reaksi kimia, berdasarkan jumlah mol reaktan atau produk.
Molaritas
Molaritas adalah jumlah mol zat terlarut dalam setiap 1 liter larutan. Konsep molaritas ini sering dikaitkan dengan stokiometri larutan.
Sekarang, untuk mengasah pemahaman Anda coba kerjakan latihan soal berikut ini!
Suatu senyawa dengan Mr = 80 mengandung 40% massa unsur X(Ar = 32) dan sisanya adalah unsur Y(Ar = 16). Tentukan rumus molekul senyawa tersebut! Tulis jawaban Anda dalam kolom komentar.
Contoh Soal Stoikiometri kelas 10
Berikut adalah beberapa contoh stoikiometri yang akan membantu memperjelas konsep dasar ini:
Contoh Soal Stoikiometri 1
Soal:
Diketahui bahwa massa 88 gram karbon dioksida (CO₂) ingin dihitung jumlah molnya. Berapa mol karbon dioksida yang terdapat dalam 88 gram gas CO₂?
Penyelesaian:
1. Langkah pertama adalah menghitung massa molar karbon dioksida (CO₂).
- Massa molar C = 12 g/mol
- Massa molar O = 16 g/mol
- Massa molar CO₂ = 12 + (2 × 16) = 44 g/mol
2. Gunakan rumus mol untuk menghitung jumlah mol:
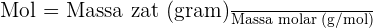
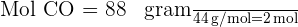
Jadi, terdapat 2 mol karbon dioksida dalam 88 gram CO₂.
Contoh Soal Stoikiometri 2
Soal:
Pada reaksi berikut:
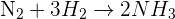
Berapa mol amonia (NH₃) yang dihasilkan jika 5 mol nitrogen (N₂) bereaksi dengan gas hidrogen (H₂) yang cukup?
Penyelesaian:
1. Langkah pertama adalah memastikan bahwa persamaan reaksi telah setara. Dari persamaan di atas, sudah jelas bahwa 1 mol N₂ bereaksi dengan 3 mol H₂ menghasilkan 2 mol NH₃.
2. Sekarang kita gunakan perbandingan mol untuk menghitung berapa banyak mol NH₃ yang dihasilkan dari 5 mol N₂. Berdasarkan persamaan reaksi, 1 mol N₂ menghasilkan 2 mol NH₃.
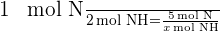
Mengalikan kedua sisi:
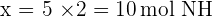
Jadi, 5 mol nitrogen akan menghasilkan 10 mol amonia.
Contoh Soal Stoikiometri 3
Soal:
Jika kita memiliki 3 mol air (H₂O), berapa massa air yang ada dalam mol tersebut?
Penyelesaian:
1. Hitung massa molar air (H₂O):
- Massa molar H = 1 g/mol
- Massa molar O = 16 g/mol
- Massa molar H₂O = (2 × 1) + 16 = 18 g/mol
2. Gunakan rumus untuk menghitung massa dari mol:
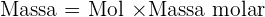
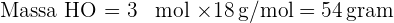
Jadi, 3 mol air memiliki massa 54 gram.
Contoh Soal Stoikiometri 4
Soal:
Berapakah volume gas oksigen (O₂) yang dihasilkan jika kita memiliki 2 mol gas oksigen pada kondisi STP?
Penyelesaian:
Pada kondisi STP (Standard Temperature and Pressure), volume gas ideal untuk 1 mol gas adalah 22,4 liter. Maka, untuk menghitung volume gas O₂, kita gunakan rumus berikut:
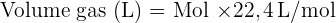
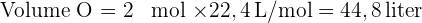
Jadi, 2 mol gas oksigen menempati volume 44,8 liter pada kondisi STP.
Contoh Soal Stoikiometri 5
Soal:
Jika suatu larutan mengandung 0,5 mol NaCl dalam 2 liter air, berapakah molaritas larutan tersebut?
Penyelesaian:
Rumus molaritas (M) adalah:

Jadi, molaritas larutan NaCl tersebut adalah 0,25 M.
Jika Anda kesulitan memahami konsep stoikiometri dan materi kimia lainnya, jangan ragu untuk mencari bantuan! Dengan tutor privat dari Superprof, Anda bisa mendapatkan bimbingan khusus yang disesuaikan dengan kebutuhan belajar Anda. Tutor-tutor berpengalaman siap membantu menjelaskan materi yang rumit dengan cara yang mudah dipahami, serta membantu Anda menguasai perhitungan kimia secara efektif. Cari tutor privat terbaik di Superprof sekarang dan tingkatkan pemahaman Anda dalam kimia!
Ringkaskan dengan AI
















